Covid-19: BioNTech y Pfizer solicitaron a regulador europeo autorización para usar su vacuna en personas entre 12 y 15 años
Las farmacéuticas explicaron que probaron en fase III su fórmula contra el coronavirus en 2.260 adolescentes, con una efectividad del 100%.
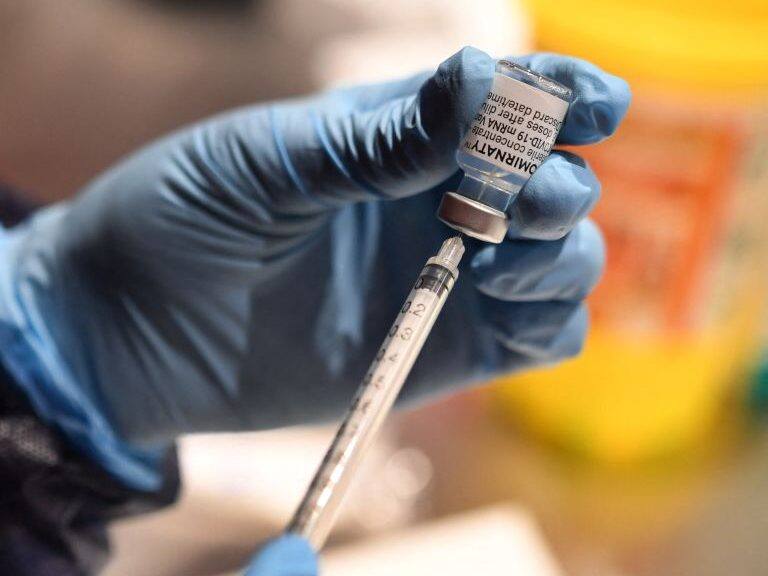
A nurse prepares a syringe with a dose of the Pfizer-BioNtech Covid-19 vaccine, at a vaccination centre in Quimper, western France, on April 30, 2021. (Photo by Fred TANNEAU / AFP) (Photo by FRED TANNEAU/AFP via Getty Images)
BioNTech y Pfizer solicitó a la Agencia Europea de Medicamentos (EMA) ampliar la autorización de su vacuna contra el covid-19 a adolescentes de entre 12 y 15 años.
En un comunicado de prensa, las farmacéuticas explicaron que probaron en fase III su fórmula contra el coronavirus en 2.260 adolescentes y que, como ya anunciaron a finales de marzo,
En las pruebas, agregan, la vacuna fue
.
[dps_related_post ids=»4785054,4769412″]
Los adolescentes participantes en la prueba
, para comprobar la protección a largo plazo de la vacuna y su seguridad.
La alemana BioNTech y la estadounidense Pfizer indican asimismo en la nota que ya han dado un paso similar en Estados Unidos, donde han pedido que se adapte su actual permiso de emergencia, y que piensan proceder de la misma forma en otras circunscripciones.








